Tous les fumeurs ne consomment pas la même quantité de cigarettes. Certains s’arrêtent à quelques-unes par jour, d’autres fument beaucoup plus. Une partie de cette différence peut être inscrite dans l’ADN. Dans une étude publiée hier sur Communications naturellesle Dr Rajagopale et ses collègues ont effectué une analyse génétique de 37 897 fumeurs Étude prospective sur la ville de Mexico et ils ont identifié une variante rare du gène CHRNB3 associé à un moins de cigarettes fumées quotidiennement. Les mêmes résultats, avec des mutations différentes mais dans le même gène, ont également été observés dans des données provenant du Royaume-Uni et du Japon. Les variantes identifiées modifier la sous-unité β3 du récepteur nicotinique, composant impliqué dans la réponse cérébrale à la nicotine : lorsque ces variants sont présents, ils sont associés à un réduction mesurable de la consommation quotidienne moyenne.
Une différence dans le gène qui pourrait réduire la consommation de cigarettes
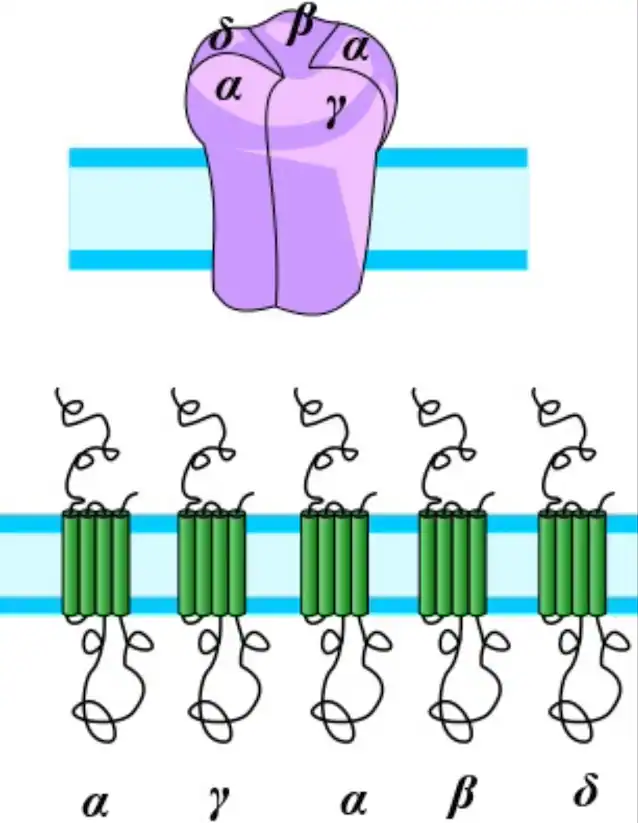
L’idée derrière l’étude est simple : si certaines personnes, en raison de leur ADN, fument spontanément moins, comprendre quelles variantes génétiques les distinguent peut aider à identifier de nouvelles cibles thérapeutiques. Le gène au centre de la recherche s’appelle CHRNB3, qui code, c’est-à-dire contient les informations nécessaires à la « construction » de la sous-unité β3 d’un récepteur présent dans le cerveau, le récepteur nicotinique de l’acétylcholine. En termes simples : c’est l’un des « verrous moléculaires » auxquels la nicotine se lie lorsqu’elle pénètre dans l’organisme. Dans des zones spécifiques du cerveau, ce lien active les circuits cérébraux liés à la récompense et à la dépendance.
Les gènes modifiés entraînent une perte d’activité de la sous-unité
En génétique, certaines variantes génétiques sont définies comme une « perte de fonction », c’est-à-dire des mutations qui réduire ou éliminer l’activité normale de la protéine.
Lorsque cela se produit dans le gène CHRNB3, la conséquence observée est une réduction de la quantité de cigarettes fumées chaque jour. Une distinction s’impose cependant : ces variantes ne semblent pas influencer de manière significative la probabilité de commencer à fumer. Ils agissent principalement surpar quantité consomméepas sur l’initiation du comportement. Ce détail suggère que la sous-unité β3 pourrait être plus impliqué dans la régulation de la dose de nicotine prise que dans le mécanisme initial de la dépendance.
Comment l’étude a été menée
Les chercheurs ont mené une analyse de l’exome, c’est-à-dire la partie de l’ADN qui contient les instructions pour fabriquer des protéines, sur 37 897 fumeurs participant actuellement à l’étude. Étude prospective sur la ville de Mexico. L’objectif était de vérifier les variantes génétiques rarec’est-à-dire présent dans moins de 1% de la population, étaient associés au nombre de cigarettes fumées chaque jour. Le résultat le plus fort concerne une variante appelée p.Glu284Gly dans le gène CHRNB3. Il s’agit d’une variante « faux-sens » : cela signifie que par rapport à la version courante de la protéine, cette variation modifie un seul acide aminé.
Cette variante p.Glu284Gly, plus fréquente chez les personnes d’ascendance indigène mexicaine, est présente dans 0,9% des participants analysésest associée à une réduction significative du nombre de cigarettes fumées par jour. L’effet est étonnamment mesurable: les non-porteurs (c’est-à-dire ceux chez qui le variant n’était pas présent) fumaient en moyenne 5,6 cigarettes par jour ; les hétérozygotes (ceux qui ne possèdent qu’une seule copie du variant) environ 4,6 cigarettes par jour (−21 %) ; homozygotes (porteurs de deux copies) environ 1,25 cigarette par jour (−78%). L’effet statistique estimé indique que ces résultats sont hautement improbable s’ils étaient simplement le résultat du hasard.
Non seulement les données du Mexique, mais aussi celles de l’Europe et du Japon
Pour vérifier que le résultat n’était pas un cas isolé au Mexique, les chercheurs ont recherché des signaux similaires dans d’autres populations. Au Royaume-Uni, l’analyse de plus de 133 000 individus du Biobanque britanniqueils ont découvert que autres variantes rares nocifs (au sens où ils entraînent une perte de fonction de la protéine, pas nécessairement nocif pour la santé) d’un même gène, considérés dans leur ensemble, sont associés à une réduction du nombre de cigarettes fumées.
Même au Japon, en Biobanque Japon (près de 75 000 individus analysés pour ce phénotype spécifique, sur les environ 180 000 présents dans la base de données), un variant différent a été identifié, mais avec un effet très similaire : une mutation qui altère la « coupure » normale de l’ARN (un variant appelé « donneur d’épissage »). En pratique, les variants réduisant ou altérant la fonction de la protéine β3 semblent être associés, dans différentes populations, à un diminution de la consommation quotidienne de cigarettes.
Comparaison avec d’autres gènes déjà impliqués
Le gène CHRNB3 n’est pas le seul à être associé au comportement tabagique. Ils étaient déjà apparus dans le passé des variantes dans d’autres régions de l’ADN, par exemple dans CHRNA5, qui fait partie du même complexe de récepteurs de nicotine, ou dans CYP2A6, qui intervient plutôt dans dégradation de nicotine dans le corps.
Le variant p.Glu284Gly identifié dans CHRNB3 produit un effet d’ampleur similaire à ceux observés pour certaines de ces mutations déjà étudiées : la réduction de la consommation quotidienne est comparable en intensitémême si le mécanisme biologique mis en jeu n’est pas forcément le même.
Vers une éventuelle cible pharmacologique
Les observations faites sont purement génétiques, mais ont des implications intéressantes : si une perte partielle de fonction est associée à une moindre consommation, la modulation pharmacologique de cette même voie pourrait produire un effet similaire. Cela ne signifie pas qu’il existe déjà un médicament capable de le faire, ni que son effet peut automatiquement être traduit en thérapie. Mais indique une direction biologique concrète: intervenir sur les récepteurs incluant la sous-unité β3 pourrait agir sur l’intensité de la consommation, c’est-à-dire sur la quantité de nicotine prise, plutôt que sur l’apparition d’un comportement tabagique.
Cependant, les chercheurs eux-mêmes soulignent certaines limites : la variante principale est spécifique à certaines populations, comme celles d’ascendance indigène mexicaine. De plus, aucune étude fonctionnelle directe n’a été menée sur la protéine altérée et l’analyse est basée uniquement sur la nombre de cigarettes fuméespas sur les diagnostics cliniques de dépendance.
